Achievements 研究成果
主な研究成果
D. Tatematsu†, N. Nakamura†, M.S. Abe‡, T. Ishikawa‡, T. Ezaki‡, L. Cai‡, E. Kawakami, K. Aihara, A. Nishida, N. Okada, N. Masuda, K. Kasai, S. Koike# and S. Iwami#, Psychological distress among Japanese high school students during the COVID-19 pandemic: An energy landscape analysis, PLOS Medicine, 23(1): e1004884 (2026). (†, ‡, # Equal contribution)
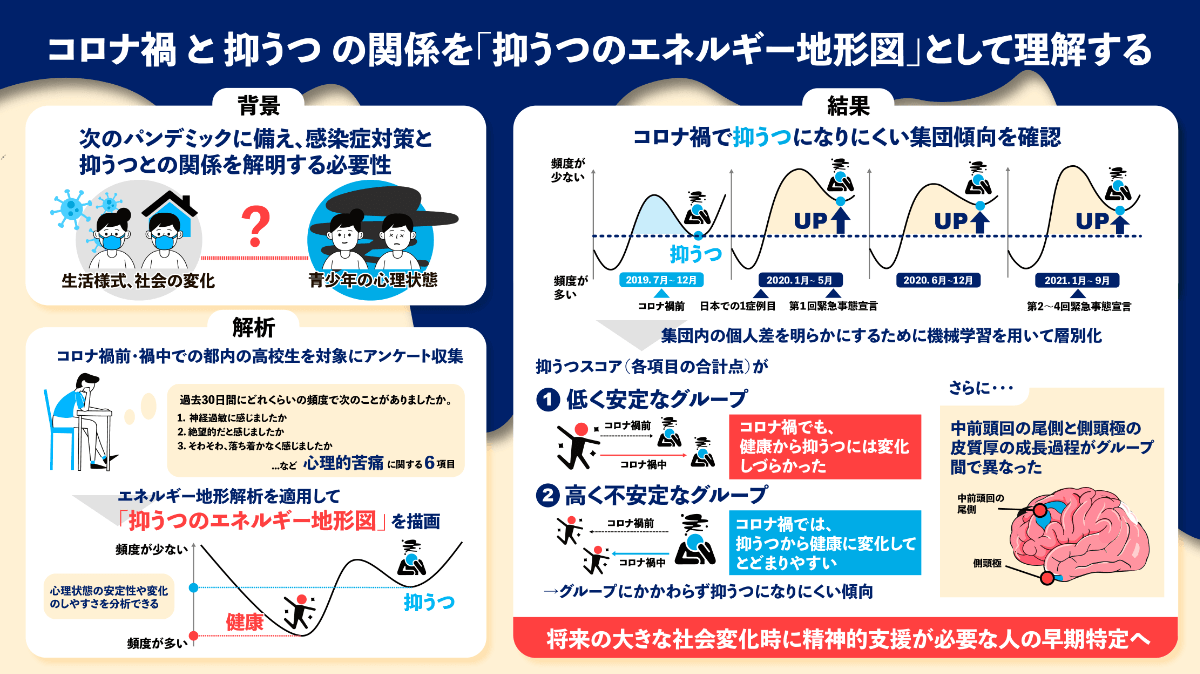
東京ティーンコホートの参加者 84 人の高校生を対象に毎月行われた抑うつに関する WEB アンケートのうち、コロナ禍前およびコロナ禍中のデータを、エネルギー地形解析を用いて解析しました。その結果、本コホートの高校生集団全体としてコロナ禍において抑うつになりにくい傾向があったことを示しました。また、層別化解析により、抑うつスコアが「低く安定なグループ」と「高く不安定なグループ」の存在を見出しました。エネルギー地形図上でシミュレーションを行った結果、コロナ禍中において、安定グループでは抑うつ状態への遷移が起こりにくく、他方、不安定グループでは健康な状態に戻りやすくなり、結果として全体の抑うつスコア平均が減少することを確認しました。さらに、アンケート調査参加者が約2年ごとに受けた頭部 MRI 検査の解析からは、中前頭回の尾側と側頭極の皮質厚の成長過程がグループ間で異なり、この脳構造の成長過程の違いが抑うつの感受性に関与している可能性も示唆しました。
- ⇒ プレスリリース(日本語)
- ⇒ プレスリリース(英語)
- ⇒ 論文
H. Park†, N. Nakamura†, S. Miyamoto, Y. Sato, K. S. Kim, K. Kitagawa, Y. Kobashi, Y. Tani, Y. Shimazu, T. Zhao, Y. Nishikawa, F. Omata, M. Kawashima, T. Abe, Y. Saito, S. Nonaka, M. Takita, C. Yamamoto, H. Morioka, K. Kato, K. Sagou, T. Yagi, T. Kawamura, A. Sugiyama, A. Nakayama, Y. Kaneko, R. Yokokawa Shibata, K. Aihara, T. Kodama, A. Kamiyama, T. Tamura, T. Fukuhara, K. Shibuya, T. Suzuki‡, S. Iwami‡ and M. Tsubokura‡, Longitudinal antibody titers measured after COVID-19 mRNA vaccination can identify individuals at risk for subsequent infection, Science Translational Medicine, 17(816):adv4214(2025). (†, ‡ Equal contribution)
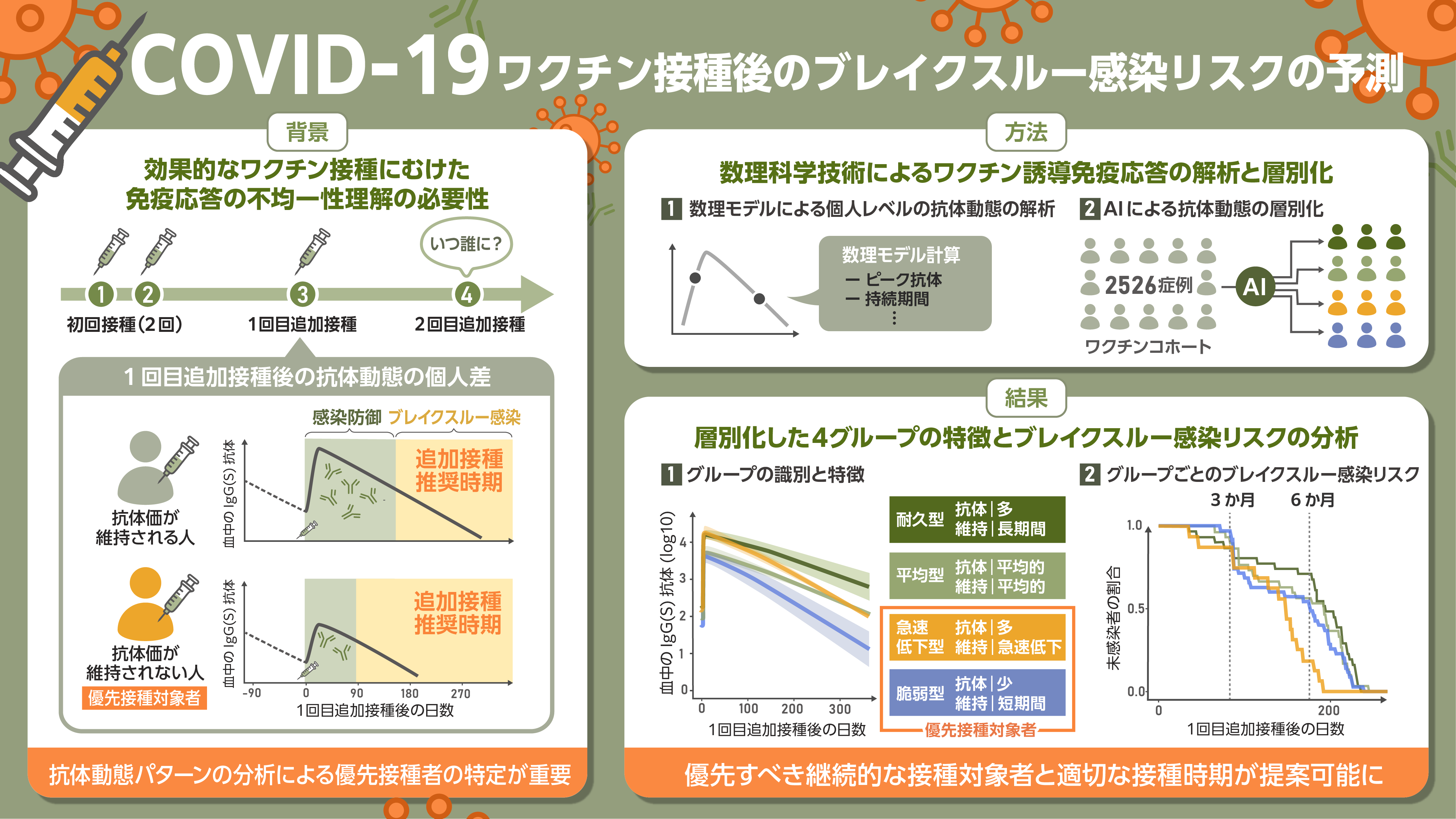
福島ワクチンコホートに参加した 2,526 名の縦断データを解析した結果、COVID-19 mRNA ワクチン追加接種後の血中 IgG(S)抗体価の推移には、「耐久型」「脆弱型」「急速低下型」という 3 種類の特徴的な応答パターンが存在することが明らかになりました。さらに、脆弱型および急速低下型に属する人々は、他の型に比べて早期にブレイクスルー感染を経験していたことも分かりました。加えて、ブレイクスルー感染を経験した人では、追加接種後 100 日以内の血中 IgA(S)抗体価が、感染を免れた人に比べて有意に低かったことが示されました。今後、このような高リスク集団を早期に特定できるようになれば、より適切なタイミングで追加接種を行うことが可能となり、感染リスクを効果的に低減できると期待されます。これは、現在流行している SARS-CoV-2 変異株や将来出現し得る新たな変異株に備える上で重要であり、社会生活の維持と感染制御を両立させる基盤となります。限られた医療資源を有効に活用し、より持続的かつ効果的なワクチン接種体制を築くためには、接種戦略の最適化が不可欠となります。なお、本研究で用いた解析手法は多様なワクチン接種に応用可能であり、その柔軟性の高さから、将来のパンデミックやポストコロナ時代における個人および集団レベルでの免疫強化政策の立案に大きく貢献すると期待されます。
- ⇒ プレスリリース(日本語)
- ⇒ プレスリリース(英語)
- ⇒ 論文
T. Nishiyama†, F. Miura†, Y.D. Jeong, N. Nakamura, H. Park, M. Ishikane, S. Yamamoto, N. Iwamoto, M. Suzuki, A. Sakurai, K. Aihara, K. Watashi, W.S. Hart, R.N. Thompson, Y. Yasutomi, N. Ohmagari, P.M. Kingebeni, J.W. Huggins, S. Iwami‡ and P.R. Pittman‡, Modeling lesion transition dynamics to clinically characterize patients with clade I mpox in the Democratic Republic of the Congo, Science Translational Medicine, 17(805): eads4773 (2025). (†, ‡ Equal contribution)
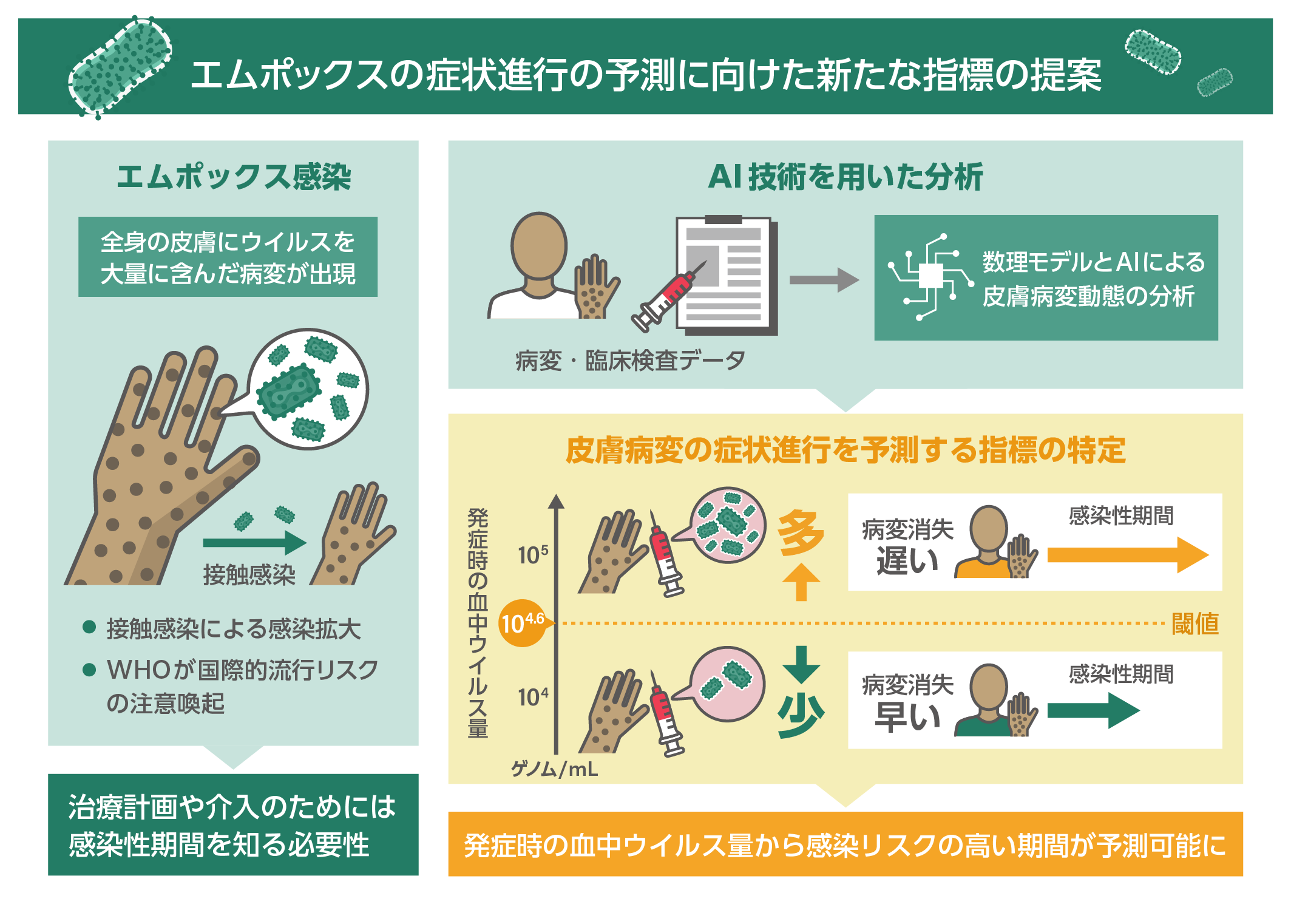
コンゴ民主共和国において 2007 年から 2011 年にかけて収集された、エムポックス(クレード Ia)感染者に関する大規模な観察研究データを数理モデルで解析し、皮膚病変の数や消失までの期間の違いに基づいて、感染者を 2 つのグループに層別化できることを示しました。さらに、各患者の血中ウイルス量の経時的変化と病変の消失時間との関係を分析した結果、病変が出現した時点の血中ウイルス量が、これら 2 グループを予測する有用な指標となることが明らかになりました。2024 年 8 月 14 日、世界保健機関(WHO)は 2 度目となる「国際的に懸念される公衆衛生上の緊急事態(PHEIC)」を宣言しました。これは、より重篤化リスクが高いとされるクレード I(Ia および Ib)の感染者数が、コンゴ民主共和国を中心に増加・拡大している現状を受けて、国際的な流行リスクへの警鐘を鳴らすものです。本研究は過去に発生したクレード Ia 感染例に基づくものですが、現在流行しているクレード Ia および Ib についても同様のデータが得られれば、皮膚病変の進行予測が可能であると期待されます。これらの知見は、今後の治療戦略の立案や公衆衛生上の介入方針の策定において、重要な科学的基盤となると考えられます。
- ⇒ プレスリリース(日本語)
- ⇒ プレスリリース(英語)
- ⇒ 論文
R. Yoshimura†, M. Tanaka†, M. Kurokawa†, N. Nakamura‡, T. Goya‡, K. Imoto, M. Kohjima‡, K. Fujiu, S. Iwami§ and Y. Ogawa§, Stratifying and predicting progression to acute liver failure during the early phase of acute liver injury, PNAS Nexus, 4(2):pgaf004 (2025). (†, ‡, § Equal contribution)
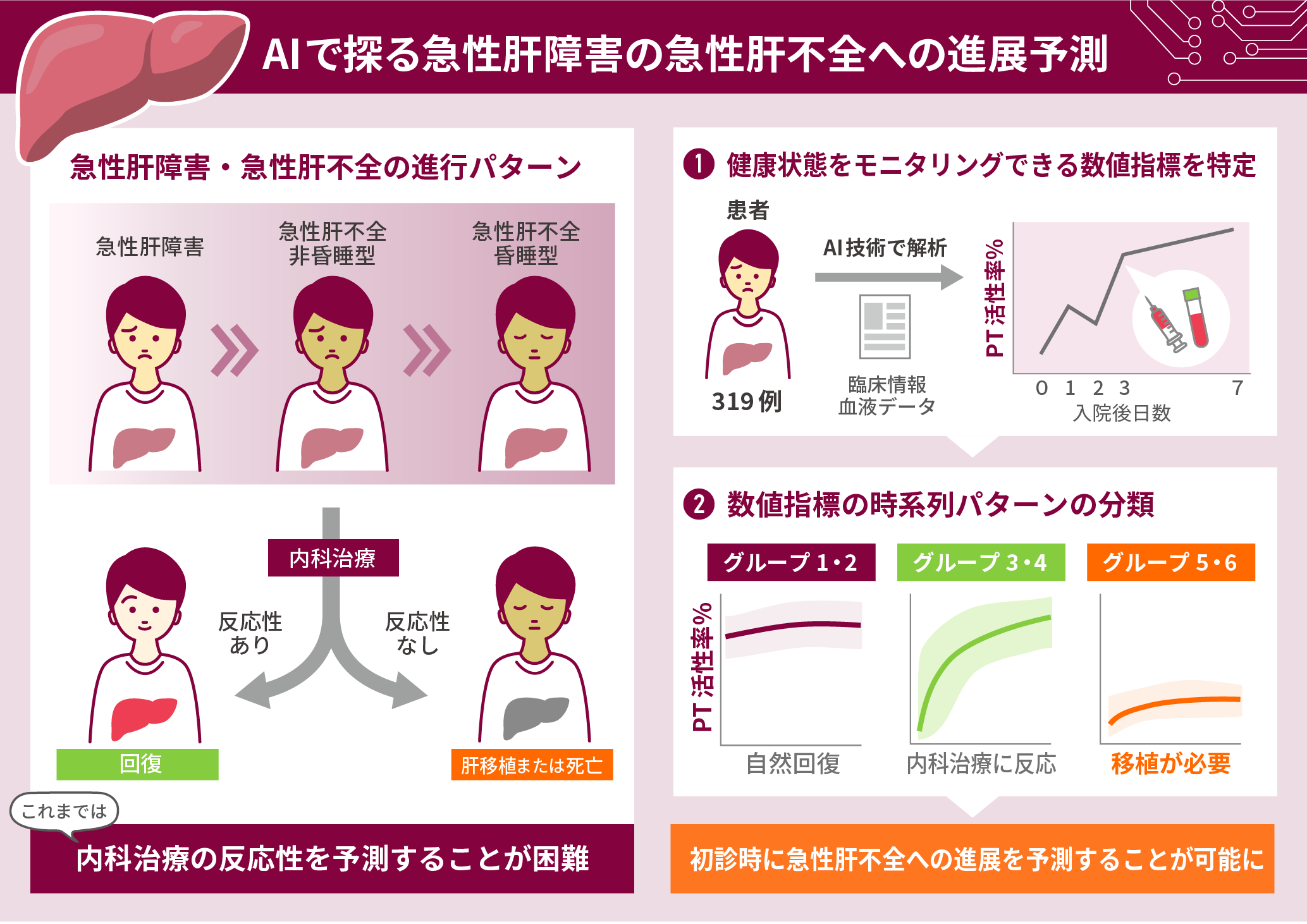
急性肝障害(ALI)および急性肝不全(ALF)の病態進行を複数のグループに層別化し、重症化を予測する新たなアプローチを開発しました。この方法により、データに基づく客観的な予後予測が可能となり、医師の臨床判断と組み合わせることで、より適切な治療が提供できるようなると期待されます。ALF は多臓器不全や死亡に至る重篤な疾患であり、ALI からの進行は個人差が大きく、ALF への移行を予測する定量的指標が不足していました。さらに、病因の多様性が重症化メカニズムの解明を困難にしていました。本研究で提案する新たな分類は、重症化機序の理解に重要な示唆を提供します。本アプローチは、入院早期から病態進行を予測し、日々の臨床情報を反映して予測精度を維持することで、個々の患者に応じた治療判断と新たな治療戦略の確立に貢献します。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
Y. D. Jeong, W. S. Hart†, R. N. Thompson†, M. Ishikane†, T. Nishiyama, H. Park, N. Iwamoto, A. Sakurai, M. Suzuki, K. Aihara, K. Watashi, E. O. de Coul, N. Ohmagari, J. Wallinga, S. Iwami‡ and F. Miura‡, Modelling the effectiveness of an isolation strategy for managing mpox outbreaks with variable infectiousness profiles, Nature Communications, 15:7112 (2024). (†, ‡ Equal contribution)
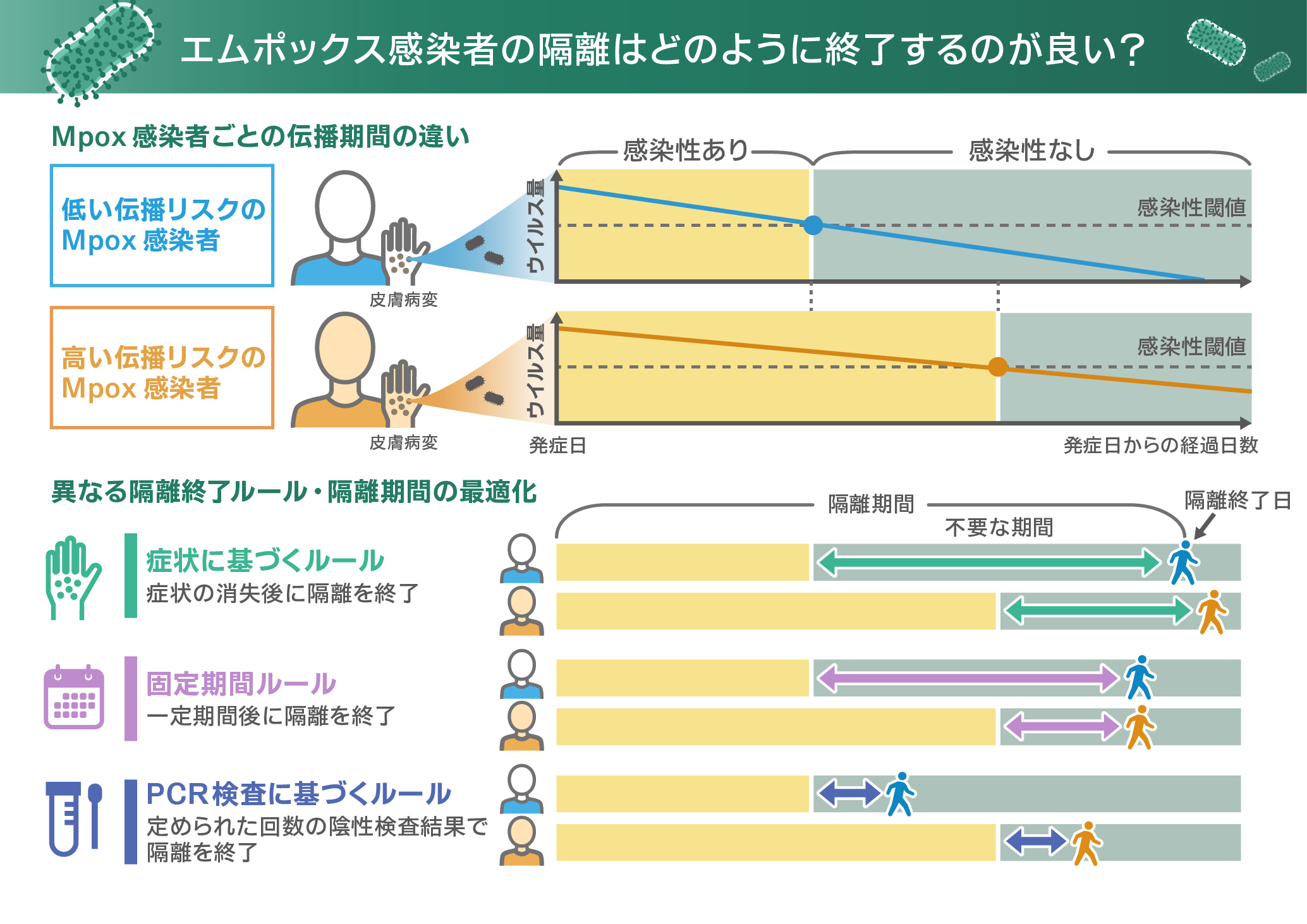
エムポックス感染者の隔離を終了するタイミングを検証するためのシミュレータを新たに開発しました。これにより、定められた回数の陰性検査結果が得られた場合に、エムポックス感染者の隔離を早期終了できる柔軟で安全な隔離戦略が提案できるようになります。2022 年 5 月以降に、新しい系統群(クレード)のエムポックスが欧米諸国を中心に国際的流行へと拡大しました。また、2024 年8月時点、コンゴ民主共和国ではより重症率の高いことが報告されている別のクレードのエムポックス感染者数が増加し、国外への流行が懸念される中、この研究は重要な示唆を提供しています。これまで新興再興感染症の発生当初においては、臨床・疫学データや経験則に基づいた異なる隔離基準が国ごとに採用されてきた状況を考慮すると、本研究は、新興再興感染症の発生初期にも、数理モデルに基づいた、世界的に求められている柔軟な隔離ガイドラインの確立に貢献できると期待されます。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
岩見真吾、中岡慎治、岩波翔也. ウイルス感染の数理モデルとシミュレーション -データを定量的に理解する-、共立出版、2024年2月.

2017 年 4 月に発売された「ウイルス感染と常微分方程式 (シリーズ・現象を解明する数学)」では、欧米諸国を中心に発展してきた“ウイルスダイナミクス”と呼ばれる数理科学とウイルス学の融合分野について、金字塔となってきた研究を中心に紹介しました。その後、2019 年 12 月、中国武漢で新型コロナウイルスが出現し、瞬く間に世界中に広がり私たちの日常を大きく変えました。今まさに、新型コロナウイルス感染症(COVID-19)を含む新興感染症に備えるためにも、現実的な問題に対応できる数理科学的なフレームワークが希求されています。そこで、本書では著者たちのオリジナル研究に基づいて、どのような数学的ツールやコードを用いればウイルス感染の数理モデルやシミュレーションが開発できるのかを解説している。特に、ウイルス学や感染症疫学、免疫学を含んだ生命医科学分野への参入を目指す数理科学を背景にする学部生・大学院生や研究者を対象に、個体群動態(数や量の時間変化)の定式化とデータ解析のノウハウを伝えている。また、本書に登場するシミュレーションはパラメータ推定を実施するためのコードは複数言語で公開しています。
- ⇒ 共立出版
S. Miyamoto†, T. Nishiyama†, A. Ueno, H. Park, T. Kanno, N. Nakamura, S. Ozono, K. Aihara, K. Takahashi, Y. Tsuchihashi, M. Ishikane, T. Arashiro, S. Saito, A. Ainai, Y. Hirata, S. Iida, H. Katano, M. Tobiume, K. Tokunaga, T. Fujimoto, M. Suzuki, M. Nakagawa, H. Nakagawa, M. Narita, Y. Kato, H. Igari, K. Fujita, T. Kato, K. Hiyama, K. Shindou, T. Adachi, K. Fukushima, F. Nakamura-Uchiyama, R. Hase, Y. Yoshimura, M. Yamato, Y. Nozaki, N. Ohmagar, M. Suzuki, T. Saito, S. Iwami# and T. Suzuki#. Infectious virus shedding duration reflects secretory IgA antibody response latency after SARS-CoV-2 infection, Proceedings of the National Academy of Sciences of the United States of America, 120(52):e2314808120 (2023). (†, # Equal contribution)
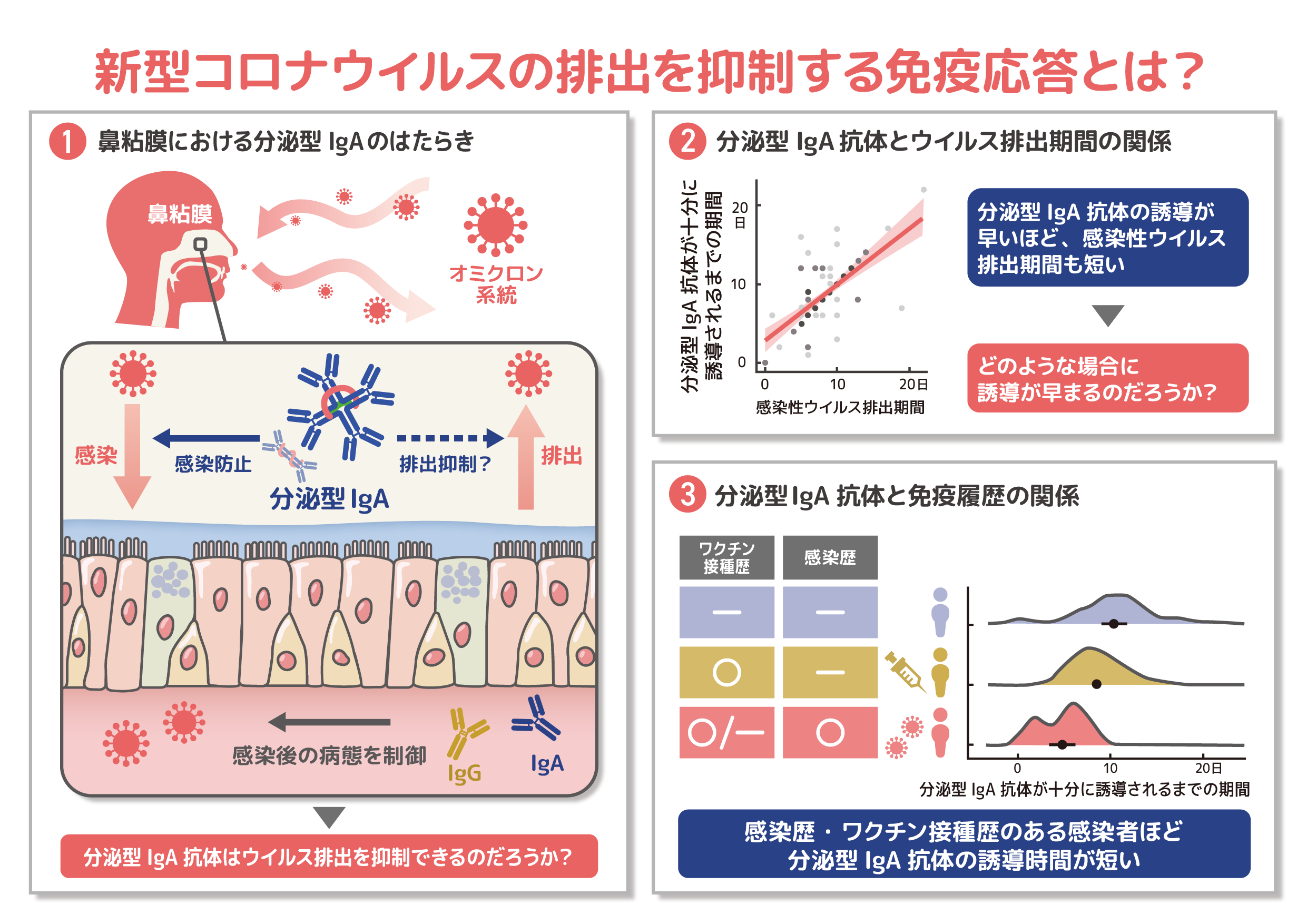
The first few hundred 調査と呼ばれる積極的疫学調査で得られたオミクロン感染者のデータと試料を倫理審査委員会の承認を得て二次利用し合計 122 人のデータを分析すると、分泌型 Ig-A(S-IgA)抗体は鼻粘膜検体において他の抗体(IgG 抗体や IgA 抗体)よりもウイルス量や感染力を強く抑制する傾向を明らかにしました。特に、粘膜表面における S-IgA 抗体の誘導が早い症例ほど感染性ウイルス排出期間が短くなりました。なお、新型コロナウイルスへの感染歴やワクチン接種歴がある感染者ほど S-IgA 抗体の誘導時間が短くなることも明らかになりました。本研究は、呼吸器ウイルス感染症において分泌型粘膜抗体が感染性ウイルス排出を抑制する可能性をヒトで示した世界で初めての報告となります。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
J. Sunagawa†, H. Park†, K. S. Kim†, R. Komorizono, S. Choi, L. Ramírez. Torres, J. Woo, Y. D. Jeong, W. S. Hart, R. N. Thompson, K. Aihara, S. Iwami# and R. Yamaguchi#. Isolation may select for earlier and higher peak viral load but shorter duration in SARS-CoV-2 evolution, Nature Communications, 14:7395 (2023). (†, # Equal contribution)
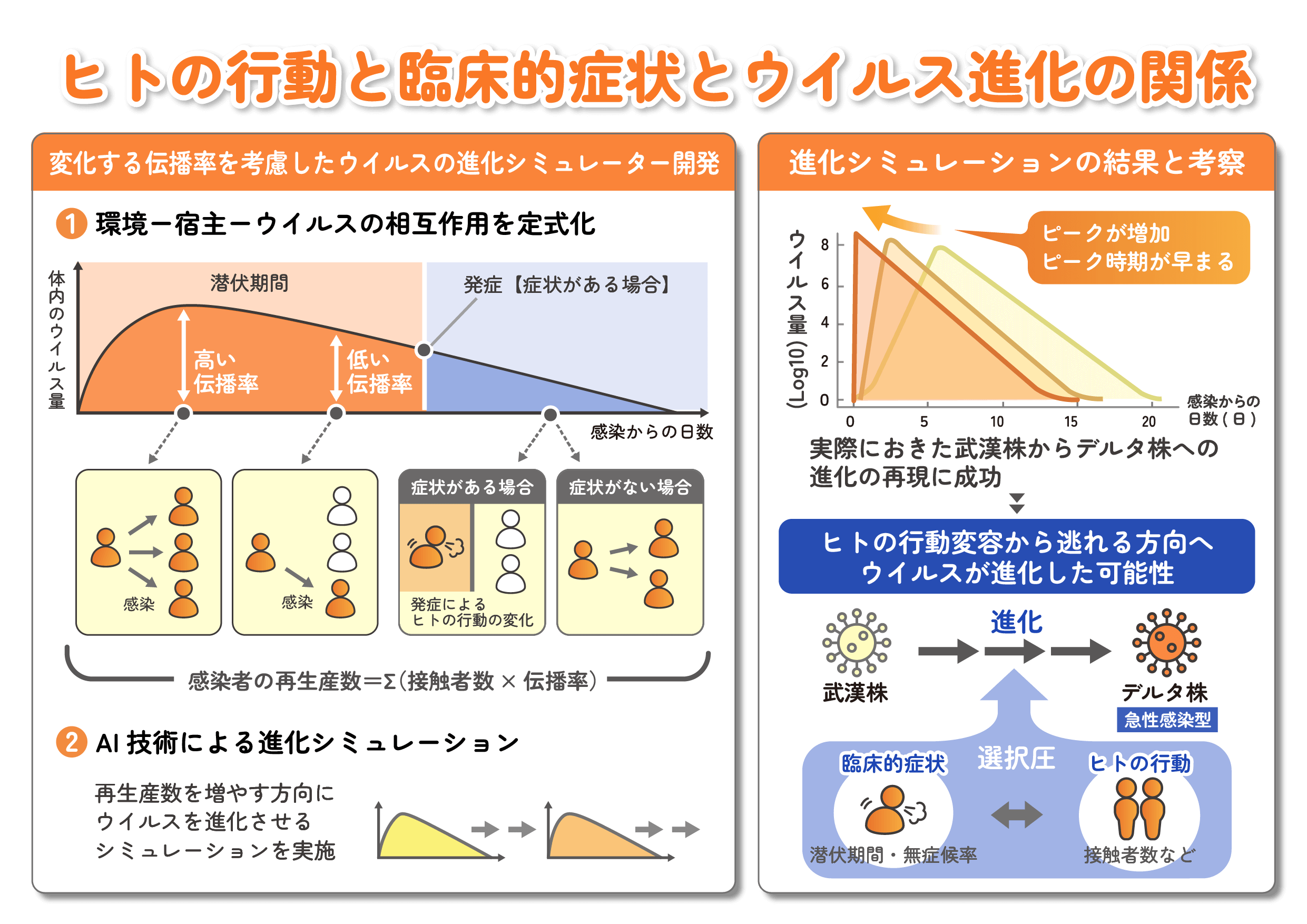
AI 技術を活用することで、新型コロナウイルスの進化が潜伏期間や無症候率などの臨床的な症状やヒトの行動と複雑に関連していた可能性を明らかにしました。武漢株、アルファ株、デルタ株、オミクロン株に感染した合計 274 人の臨床データを順番に解析していくと、変異株の出現に伴い、生体内におけるウイルス排出量のピークは増加し、早まる傾向(急性感染型)に進化する様子が見られました。さらに、AI 技術を組み込んだシミュレータを開発し、詳細に分析した結果、この進化の傾向は、変異株の出現に応じてヒトが感染症から身を守るための行動(自宅待機、3密回避、感染者隔離など)を克服するウイルスの生存戦略として成立したものである可能性が示唆されました。また、変異株の出現とともに短くなった潜伏期間や高くなった無症候率も、変異株を進化させる選択圧と密接に関連していることが判明しました。本研究により、ヒトの行動自体もウイルスの進化を理解する上で重要な原因であることが明らかになりました。
- ⇒ プレスリリース(日本語)
- ⇒ プレスリリース(英語)
- ⇒ 論文
W. S. Hart, H. Park, Y. D. Jeong, K. S. Kim, R. Yoshimura, R. N. Thompson† and S. Iwami†, Analysis of the risk and pre-emptive control of viral outbreaks accounting for within-host dynamics: SARS-CoV-2 as a case study, Proceedings of the National Academy of Sciences of the United States of America, 120(41):e2305451120 (2023). († Equal contribution)
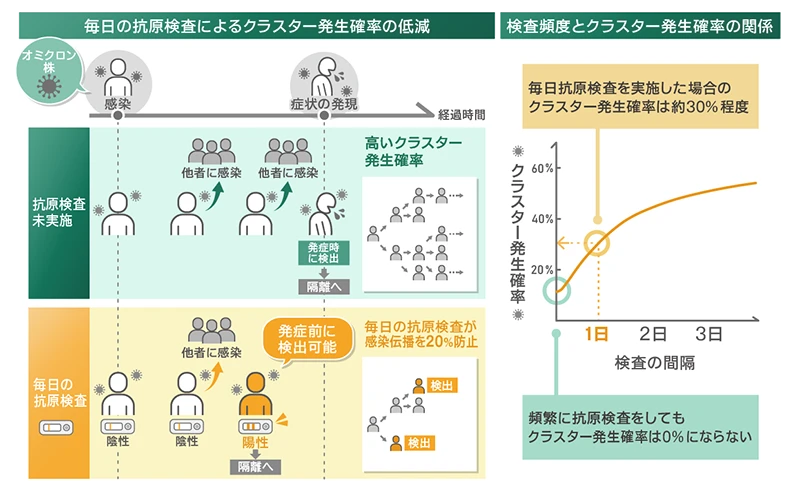
感染者ごとのウイルス排出動態の個人差を考慮した上で、新型コロナウイルス感染によるクラスターの発生確率の計算に世界ではじめて成功しました。この画期的な方法により、感染者ごとに異なるウイルス量の時間変化を分析し、抗原検査や抗ウイルス薬剤による治療の個別介入を行うことで、クラスターの発生確率に及ぼす影響を評価することが可能になりました。この手法によれば、抗原検査による感染者スクリーニングは、クラスターの発生確率を大幅に低減する効果がありますが、感染力の強い変異株(例: オミクロン株)によるクラスターを完全に防ぐことは難しいことが明らかになりました。クラスター発生のリスクを最小限に抑える必要がある状況下で、本研究の成果は、数理モデルに基づく効果的な感染症対策の確立に向けた重要な一歩となることが期待されます。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
Y.D. Jeong†, K. Ejima†, K.S. Kim†, J. Woo, S. Iwanami, Y. Fujita, IH. Jung, K. Aihara, K. Shibuya, S. Iwami, A.I. Bento and M. Ajelli, Designing isolation guidelines for COVID-19 patients with rapid antigen tests, Nature Communications, 13:4910(2022). (†Equal contribution)
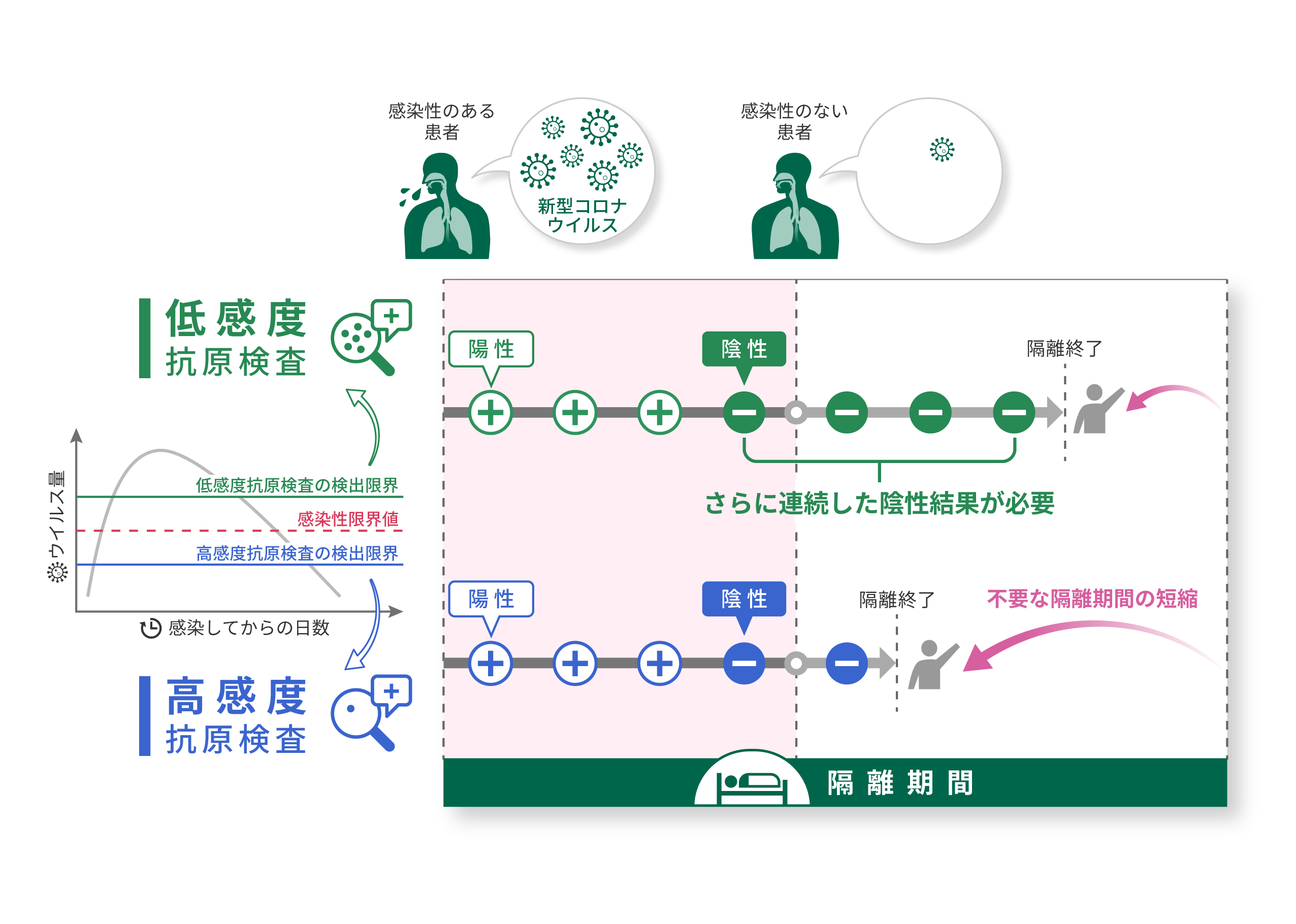
決められた回数の抗原検査の陰性結果をもって、早期に COVID-19 感染者の隔離を終了できる、柔軟で安全な隔離戦略を検証するためのシミュレータを新たに開発しました。感染者隔離は感染拡大を防ぐ重要な手段ですが、長期にわたる隔離は二次感染のリスクを下げる一方で、隔離される人やそれを支える社会も様々な負担を被ります。感染予防対策を徹底しつつ社会活動を再開・維持するウィズコロナの時代を迎えるにあたり、抗原検査をうまく利用することで教育活動や社会活動を安全に実施することが期待されています。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
Y. D. Jeong†, K. Ejima†, K. S. Kim†, S. Iwanami, A. I. Bento, Y. Fujita, I. H. Jung, K. Aihara, K. Watashi, T. Miyazaki, T. Wakita, S. Iwami, M. Ajelli. Revisiting the guidelines for ending isolation for COVID-19 patients, eLife, 10:e69340 (2021). (†Equal contribution)
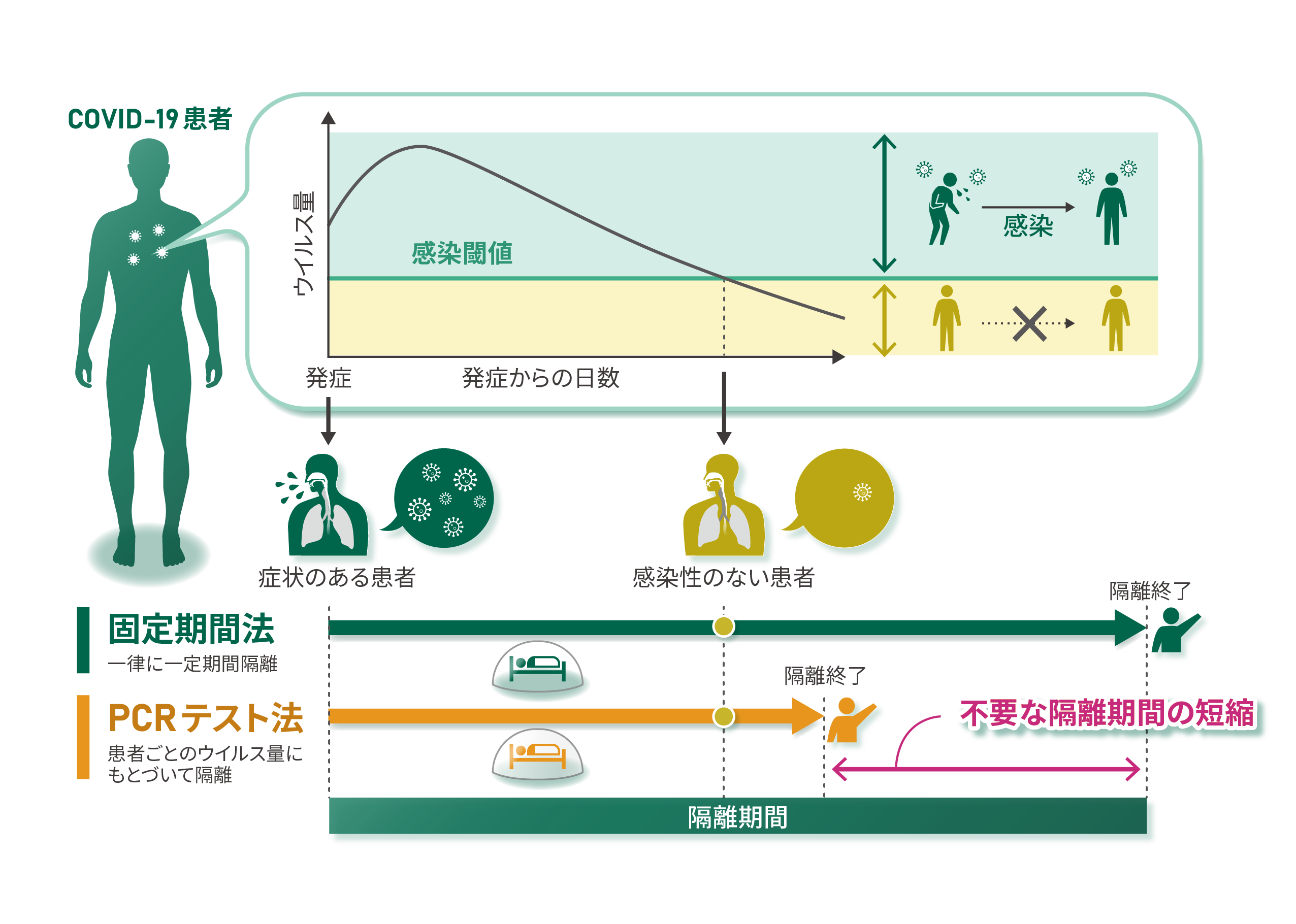
新型コロナウイルス(COVID-19)感染者の隔離を終了するタイミングを検証するためのシミュレータを新たに開発しました。このシミュレータを用いれば“感染性のある患者の隔離を(早く)終了してしまうリスク”と“感染性を失った患者を不要に隔離してしまう期間(隔離に関わる負担)”が計算できます。この結果、リスクと負担を同時に抑えるための適切な隔離戦略を(PCR テストが十分にできるかなど)状況に応じて提案できるようになりました。現在、経験則に基づいた異なる隔離基準が国ごとに採用されている状況に対して、本研究は、科学的根拠に基づいた隔離ガイドラインの確立に貢献できると期待されます。
- ⇒ プレスリリース(日本語)
- ⇒ プレスリリース(英語)
- ⇒ 論文
S. Iwanami†, K. Ejima†*, K.S. Kim, K. Noshita, Y. Fujita, T. Miyazaki, S. Kohno, Y. Miyazaki, S. Morimoto, S. Nakaoka, Y. Koizumi, Y. Asai, K. Aihara, K. Watashi, R. N. Thompson, K. Shibuya, K. Fujiu, A.S. Perelson‡, S. Iwami‡*, T. Wakita. Detection of significant antiviral drug effects on COVID-19 with reasonable sample sizes in randomized controlled trials: A modeling study, PLOS Medicine, 18(7):e1003660 (2021). (†,‡Equal contribution)
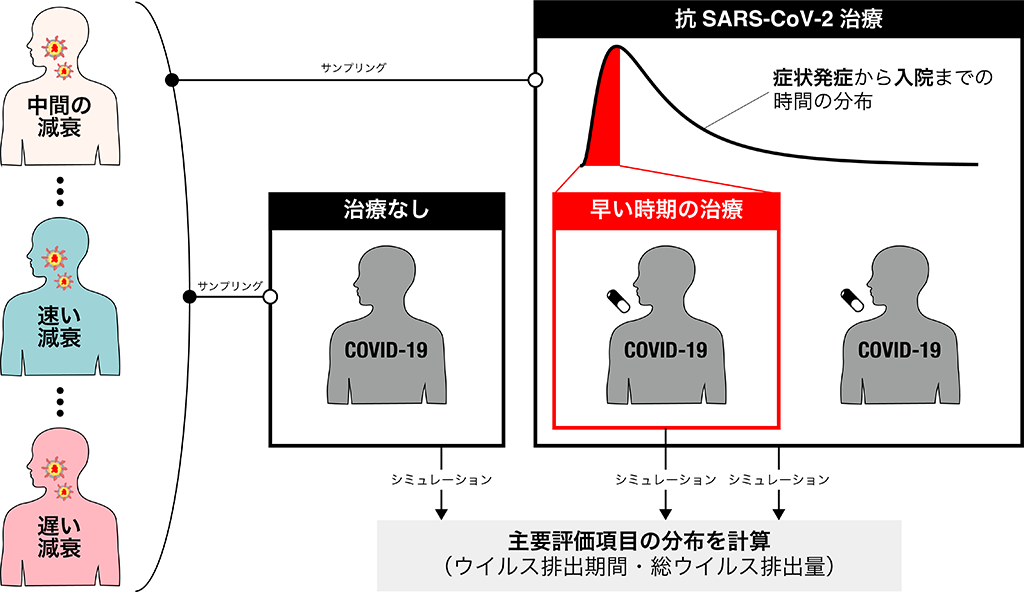
新型コロナウイルス感染症(COVID-19)に感染した場合、ウイルス排出量が短期(発症 7 日程度)、中期(発症 14 日程度)、長期(発症 28 日程度)の3グループに層別化できることが明らかにしました。また、全てのグループにおいて、ウイルス複製阻害薬剤やウイルス侵入阻害薬剤による治療開始時期が、ウイルス排出量のピークの前か後かで、ウイルス排出量を減少させる効果が大きく異なることを示しました。つまり、COVID-19 症例では、個人個人でウイルス排出量がばらばらで、また、治療開始時期に応じてそれら排出量への効果が異なってきます。そして、このような極めて不均一な特徴をもつ症例に対して、抗ウイルス薬剤の効果を臨床試験において正しく評価するためのシミュレータ(in silico randomized clinical trial: isRCT)の開発を行い、一部 isRCT を用いてデザインされた医師主導治験(jRCT2071200023)が日本で行われております。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
K. S. Kim†, K. Ejima†, S. Iwanami, Y. Fujita, H. Ohashi, Y. Koizumi, Y. Asai, S. Nakaoka, K. Watashi, K. Aihara, R. N. Thompson, R. Ke, A. S. Perelson‡ and S. Iwami‡. A quantitative model used to compare within-host SARS-CoV-2, MERS-CoV and SARS-CoV dynamics provides insights into the pathogenesis and treatment of SARS-CoV-2, PLOS Biology, 19(3):e3001128. (2021). (†,‡Equal contribution).
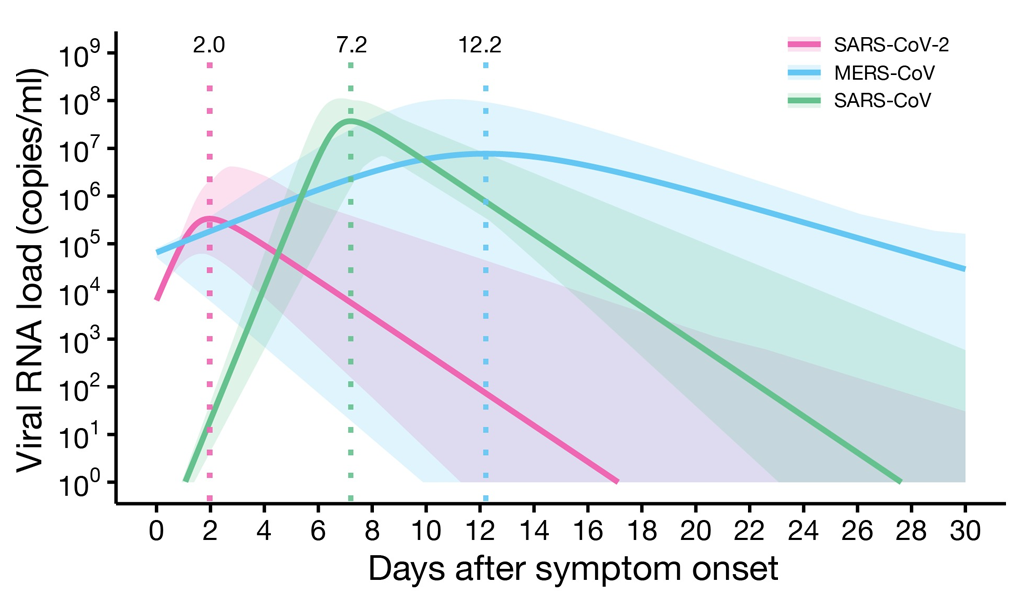
新型コロナウイルス感染症(COVID-19)に対する抗ウイルス薬剤治療が他のウイルス感染症と比較して困難である理由の1つを解明しました。インフルエンザなどの臨床試験からも知られている通り、一般的にウイルス排出量がピークを迎える前にウイルス複製阻害薬剤の投与を開始することが、排出量を減少させるために重要です。COVID-19 に加えて過去に流行した中東呼吸器症候群(MERS)および重症急性呼吸器症候群(SARS)の臨床試験データを収集・分析すると、COVID-19 では過去のコロナウイルス感染症である MERS や SARS と比較して、早期にウイルス排出量がピークに達することが明らかになりました。また、開発したコンピュータシミュレーションによる網羅的な分析によると、たとえ使用するウイルス複製阻害薬剤やウイルス侵入阻害薬剤が強力であったとしても、ピーク後に治療を開始した場合、ウイルス排出量を減少させる効果は極めて限定的であることを見出しました。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
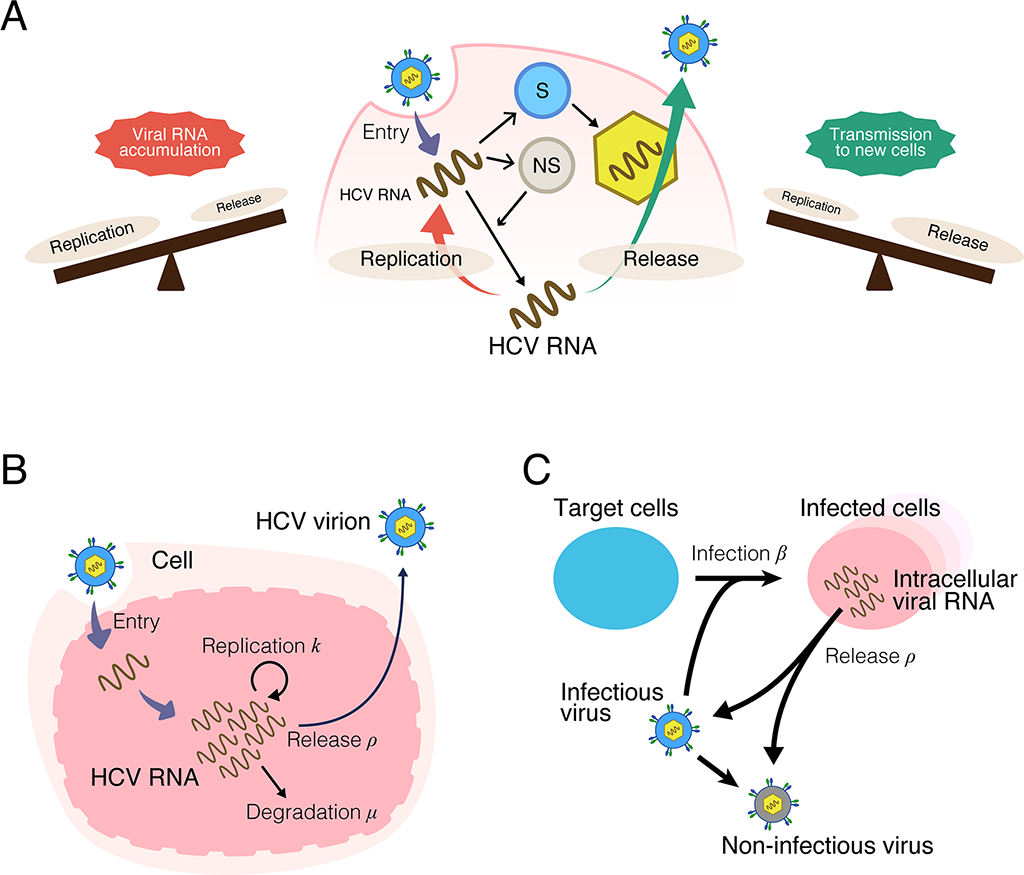
S. Iwanami, K. Kitagawa, H. Ohashi, Y. Asai, K. Shionoya, W. Saso, K. Nishioka, H. Inaba, S. Nakaoka, T. Wakita, O. Diekmann, *S. Iwami†, *K. Watashi†. Should a viral genome stay in the host cell or leave? A quantitative dynamics study of how hepatitis C virus deals with this dilemma, PLOS Biology, 18:e3000562 (2020). (†Equal contribution/Corresponding author).
ウイルスがもつ「細胞中に引きこもって、安全に子孫を複製する」か「粒子として危険を冒して外出し、別の細胞に感染し増殖する」かの2つの戦略の存在を世界で初めて証明した実験・理論の融合研究です。細胞内・外のウイルス生活環を統一的に記述する多階層数理モデルを開発することで、感染実験から計測される多階層データの定量的分析が可能になった点は特筆すべきです。
- ⇒ プレスリリース(日本語)
- ⇒ プレスリリース(英語)
- ⇒ JST 記事
- ⇒ 論文
M. Mahgoub, J. Yasunaga, S. Iwami, S. Nakaoka, Y. Koizumi, K. Shimura, M. Matsuoka. Sporadic on/off switching of HTLV-1 Tax expression is crucial to maintain the whole population of virus-induced leukemic cells, Proceedings of the National Academy of Sciences of the United States of America, 115(6):E1269-E1278 (2018).
高免疫原性の HTLV-1 の tax 遺伝子発現が間歇的であることを 1 細胞ライブイメージングにより発見し、tax 遺伝子発現は感染細胞が抗アポトーシス耐性を獲得するために必須であることを示しました。また、モデル駆動型の定量的データ解析により間歇的な tax 遺伝子発現が細胞集団全体の生存を維持していることを見出しました。感染細胞が免疫細胞から逃れつつ、抗アポトーシス耐性を獲得するためにウイルス遺伝子発現をオン・オフと調節しながら機能していることを明らかにした初めての研究です。
- ⇒ プレスリリース(英語)
- ⇒ 論文
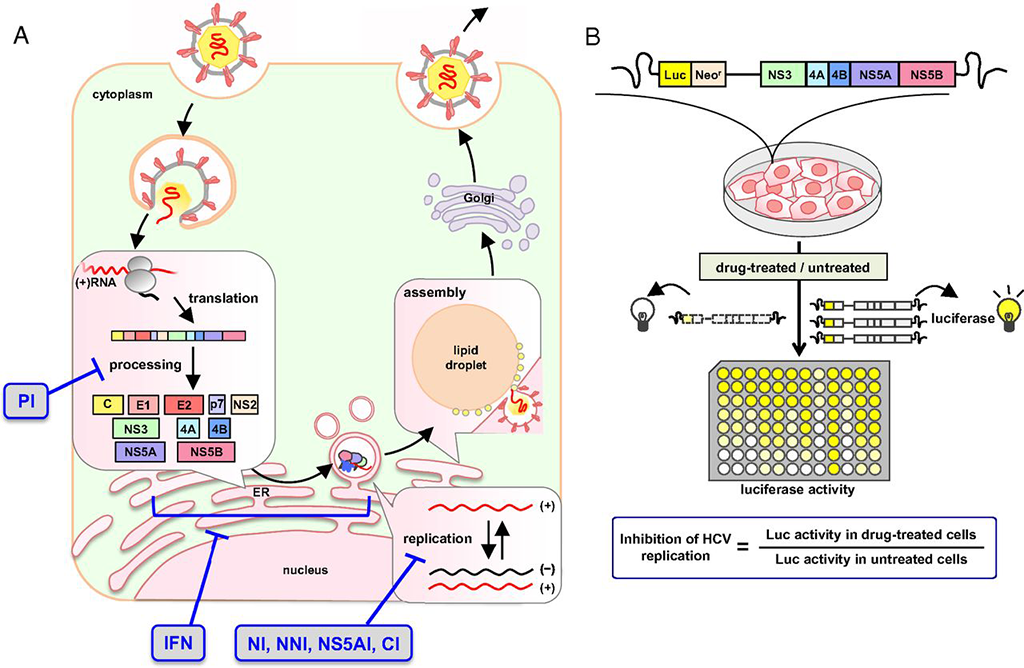
Y. Koizumi, H. Ohashi, S. Nakajima, Y. Tanaka, T. Wakita, AS. Perelson, *S. Iwami†, *K. Watashi†. Quantifying antiviral activity optimizes drug combinations against hepatitis C virus infection, Proceedings of the National Academy of Sciences of the United States of America, 114: 1922-1927 (2017). (†Equal contribution/Corresponding author)
レプリコンシステムにより抗 HCV 薬剤効果を簡便かつハイスループットに計測する方法を確立しました。また、確立した手法と数理モデルを融合させることで、ウイルス抑制効果と耐性株出現確率を最適化する抗 HCV 薬の組み合わせを網羅的に分析した初めての研究です。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
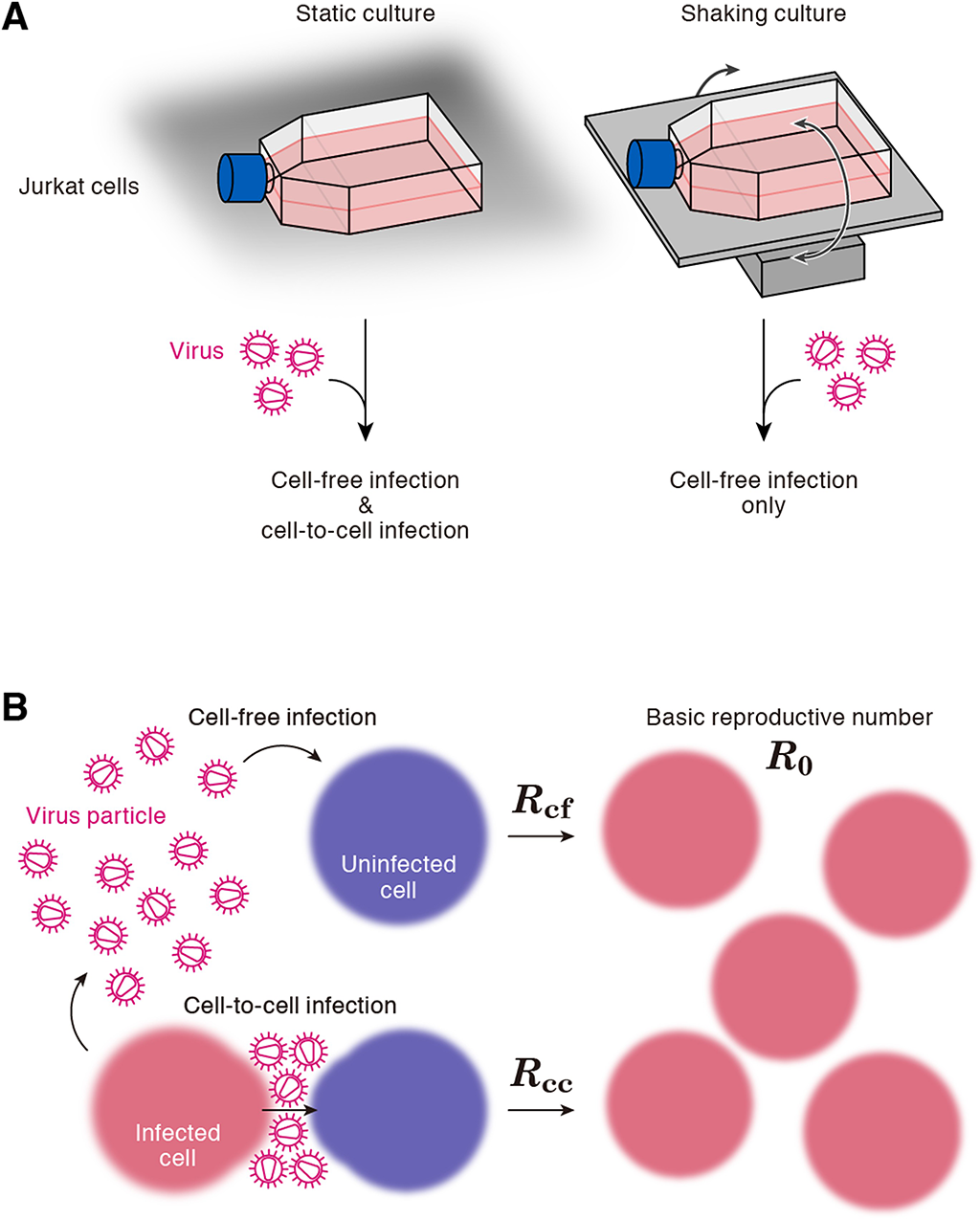
*S. Iwami†, JS Takeuchi†, S Nakaoka, F Mammano, F Clavel, H Inaba, T Kobayashi, N Misawa, K Aihara, Y Koyanagi, *K Sato. Cell-to-cell infection by HIV contributes over half of virus infection, Elife, 4, (2015). (†Equal contribution/Corresponding author)
HIV が有する cell-to-cell 感染と cell-free 感染の2つの感染モードを記述する数理モデルを開発しました。また、理論的にデザインされた感染実験より取得した経時的データを数理モデルで解析することで、cell-to-cell 感染が全感染の 60%以上を担っていることを明らかにした初めての研究です。
- ⇒ プレスリリース(日本語)
- ⇒ 論文
岩見真吾、佐藤佳、竹内康博. シリーズ現象を解明する数学 「ウイルス感染と常微分方程式」、共立出版、2017年4月.

本書は,常微分方程式の数理モデルに焦点を当て,歴史的に重要な論文と著者らのオリジナル研究を紹介する日本初のウイルスダイナミクスの入門書です。欧米諸国を中心に繰り広げられてきた数理モデルを用いた臨床データの定量的解析および,著者らが近年展開している数理モデルを用いたウイルス感染実験データの定量的解析を詳細に説明しています。また,本書で解析される様々なウイルス感染の実験データもすべて掲載しています。
- ⇒ 共立出版